在蛋白质合成过程中,有一些酶能够将氨基酸附着到转运RNA上;它们必须能够特异性地识别氨基酸和转运RNA这两种底物。这些酶的晶体结构揭示了一个特殊的机制,可以解释为什么此类催化系统的RNA识别具有特异性。
几十年以来,研究者们一直都痴迷于这样一个问题:核酸编码的遗传信息是如何被翻译成蛋白质氨基酸序列的呢?精确的翻译过程包括:信使RNA上被称为密码子(codon)的核苷酸三联体与转运RNA上相互补的反密码子(anticodon)进行特异性的互补配对。翻译过程的高精确性也要求要将每种类型的氨基酸精确地附着到(即氨酰化)特定的tRNA上。所有不同类型的氨酰化反应都是在一种特殊酶的催化作用下进行的,即氨酰tRNA合成酶(aminoacyl-tRNA synthetase, ARS);这种酶必须能够从众多类似的底物中区分出哪些是自己的氨基酸底物,而哪些是能与之匹配的tRNA。近日,Naganuma等人报道了ARS酶的晶体结构,使研究者们终于明白,ARS到底是通过何种不同寻常的机制来解释tRNA部分区域上编码的遗传信息,最终催化高度特异性的氨酰化反应的。
最简单的tRNA识别是丙氨酰tRNA合成酶(alanyl-tRNA synthetase, AlaRS)的tRNA识别,这种酶能够将丙氨酸附着到相应的tRNA(tRNAAla)上。在所有的生命体中,这种识别过程主要依赖于一个被命名为G3∙U70(其中G和U分别表示鸟嘌呤和尿嘧啶)的“摆动”碱基对,这个碱基对存在于tRNAAla上一个被称为氨基酸接纳茎(acceptor stem)的区域中。长久以来,AlaRS-tRNA系统一直都是研究蛋白质-RNA交互作用的实验模型,并且已经得到了广泛的研究。我们从此类研究中了解了很多东西,也通过研究其他大多数ARS∙tRNA复合物的立体结构,掌握了一些相关情况,但是却一直没有对AlaRS-tRNAAla复合物的晶体结构进行研究。如今,Naganuma等人报道了闪烁古生球菌(Archaeoglobus fulgidus)中AlaRS与tRNAAla/GU(即含有G3∙U70摆动碱基对的野生型tRNA)形成复合物时的晶体结构,也报道了AlaRS与tRNAAla/AU,即在摆动碱基对的位置上含有一个标准的沃森-克里克碱基对(Watson-Crick pair)的突变型tRNAAla形成缺陷性复合物时的晶体结构。
有一些核苷酸被称为tRNA识别元件,它们能够标记tRNA,以便对其进行特定的氨酰化反应,而研究者们已经充分了解了细菌内tRNA合成酶系统中所有的tRNA识别元件。除了邻近于氨基酸附着位点的接纳茎区域以外,反密码子对于大多数tRNA而言也是其中一类识别元件。近年来研究者们发现,G3∙U70碱基对在AlaRS识别过程中具有重要的作用,而AlaRS酶无法识别反密码子。这些结论有助于我们解释早期的研究发现——来源于接纳茎的tRNAAla片段是AlaRS催化氨酰化反应的底物。此外,这些结论也引起了研究者们的猜测:“第二遗传密码”可能决定了氨基酸在tRNA分子上的特异性附着。
研究者们随后又观察到,用沃森-克里克碱基对替换摆动碱基对后,将会大大降低AlaRS的tRNAAla氨酰化催化速率(rate of catalysis, kcat),但是并不会影响tRNAAla与AlaRS的结合能力。此外,以下两种情况同样也会影响AlaRS的识别过程:G3∙U70碱基对的内部及其周围存在有特定的化学基团,或者tRNAAla的螺旋形接纳茎发生了扭曲。这些研究结果给我们留下了一个疑问:AlaRS是如何通过影响kcat来完成识别过程的呢?
Naganuma等人所报道的晶体结构显示,AlaRS可形成同源二聚体(由两个相同的酶亚基连接而成),而每个同源二聚体都可以结合一个分子的tRNA。一个AlaRS亚基可分为四个区域,而tRNA可以以一种闻所未闻的定向,与其中的三个区域相互作用。AlaRS酶的羟基末端结构域通过与L形tRNA的“肘状角”区域相互作用,从而结合到tRNAAla/GU上,而其氨酰化区域则与tRNA的3ʹ-CCA末端(即含有丙氨酸附着点的3’端单链区域)相互作用。
RNA分子的双链区域(例如tRNAAla的接纳茎)含有两道被称为大沟(major groove)和小沟(minor groove)的凹沟。Naganuma等人报道指出,tRNAAla/GU接纳茎的识别过程是由两个α-螺旋(即α11与α14,位于AlaRS的tRNA识别区域)的末端来介导的,这两个α-螺旋能够紧紧地抓住接纳茎,并同时夹住小沟和大沟,从而将接纳茎定位到合适的区域上,以便进行氨酰化反应。α11和α14强大的夹紧力能够使接纳茎上的大沟变宽,从而防止AlaRS的其他区域在结构上产生冲突。
Naganuma等人也发现,G3∙U70碱基对呈现出摆动的几何结构,其中G3朝向小沟。G3的氨基似乎能够与α14上天冬氨酸的氨基酸残基(Asp 450)之间形成两个氢键,这就支持了以下观点:即这个基团在AlaRS催化氨酰化反应的过程中发挥了关键作用。相对于其它已被确定的ARS∙tRNA复合物中游离的tRNA而言,ARS-tRNAAla复合物中tRNAAla的L形结构只是受到了较轻微的扭曲。
总体而言,Naganuma等人所发现的晶体结构显示,AlaRS采用相似的方式来适应tRNAAla/AU和tRNAAla/GU的结构,但是他们也揭示了一个前所未知的机制,G3∙U70摆动碱基对的局部几何结构正是通过这一机制“穿过“双链接纳茎,最终被传递到3ʹ-CCA单链区域中。在含有GU的复合物中,3ʹ-CCA末端(即氨基酸附着位点)能够结合到AlaRS的活性位点上(图1)。但是在含有AU的突变型复合物中,3ʹ-CCA末端发生弯曲,将会偏离AlaRS活性位点。3ʹ-CCA末端附近的核苷酸之间的相互作用可能能够稳定这种弯曲的构象。从原则上而言,tRNAAla/AU能够在平直构象和弯曲构象之间自由转换,但是即便如此,这种构象上的变化也会被AlaRS上一个类似“路线分隔器”的特殊结构所限制;这一结构由三个连续排列的甘氨酸氨基酸残基以及一个谷氨酸氨基酸残基组成。
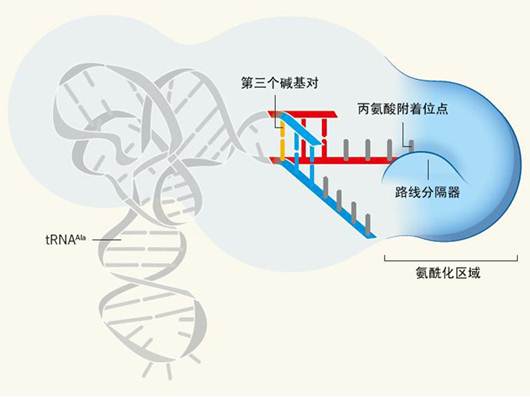
图1 | 转运RNA上单个碱基对对构象的影响。AlaRS酶能够使丙氨酸附着(即氨酰化)到与之匹配的tRNA上(tRNAAla)。Naganuma等人报道了AlaRS与野生型tRNAAla(在螺旋状接纳茎的第三个碱基对位点上含有一个“摆动”碱基对)形成复合物时的晶体结构,也报道了AlaRS与突变型tRNAAla(在同一个位置上含有一个沃森-克里克碱基对,而不是摆动碱基对)形成复合物时的晶体结构。在这幅图中,阴影部分表示AlaRS上与tRNA相连接的区域。Naganuma等人发现,当存在有摆动碱基对时,tRNAAla的接纳茎区域将会采用平直的构象(红色),但是当同一位置上的摆动碱基对被沃森-克里克碱基对替换时,接纳茎则会呈现出弯曲的构象(蓝色)。只有平直的构象才能够将RNA的单链区域牵引到AlaRS的氨酰化区域中。氨酰化区域中的氨基酸残基就像一个“路线分隔器”,可以防止两个构象之间发生相互转换。
Naganuma等人采用动力学分析,证实闪烁古生球菌内的AlaRS二聚体在催化tRNAAla/GU的氨酰化反应时,其kcat值比催化tRNAAla/AU时的kcat值高100倍左右,而两者之间的氨酰化产物生成率以及与突变型tRNA的结合能力却只相差两倍左右。因此,AlaRS对tRNA的识别过程似乎依赖于一种特殊的催化机制,而这种机制则取决于AlaRS结合的tRNA是处于“活性”状态(即平直的接纳茎),还是处于“无活性”状态(即弯曲的接纳茎)。
尽管Naganuma等人的研究发现提供了一些振奋人心的信息,让研究者们了解了AlaRS区分tRNAAla/GU和tRNAAla/AU的机制,但是我们仍然需要获得分辨率更高的晶体结构,以便于使特异性氢键结合作用具有更高的可信度。此外,我们目前仍然不清楚AlaRS是如何识别线粒体tRNAAla分子的,因为这些tRNAAla分子通常都没有G3∙U70碱基对。我们也尚不清楚tRNAAla/GU的3ʹ-CCA末端是如何与AlaRS上第二个催化位点(即编辑区域)相互作用的,这个催化位点能够水解tRNA,进而可以附着错误的氨基酸;此外,该位点也能够识别G3∙U70碱基对。
我们还需要分析其它与突变型tRNA相连接的ARS的晶体结构,来确定这些酶是否也存在活性状态和无活性状态,是否也利用路线分隔器,从而来解码其各自的识别元件。最后,还有其他一些将G∙U摆动碱基对作为特异性识别信号的RNA是否也会采用相类似的机制呢,让我们拭目以待!
原文检索:
Oscar Vargas-Rodriguez& Karin Musier-Forsyth. Structural biology: Wobble puts RNA on target. Nature, 11 June 2014; doi:10.1038/nature13502
转载原文出处:http://www.bio360.net/news/show/10765.html






